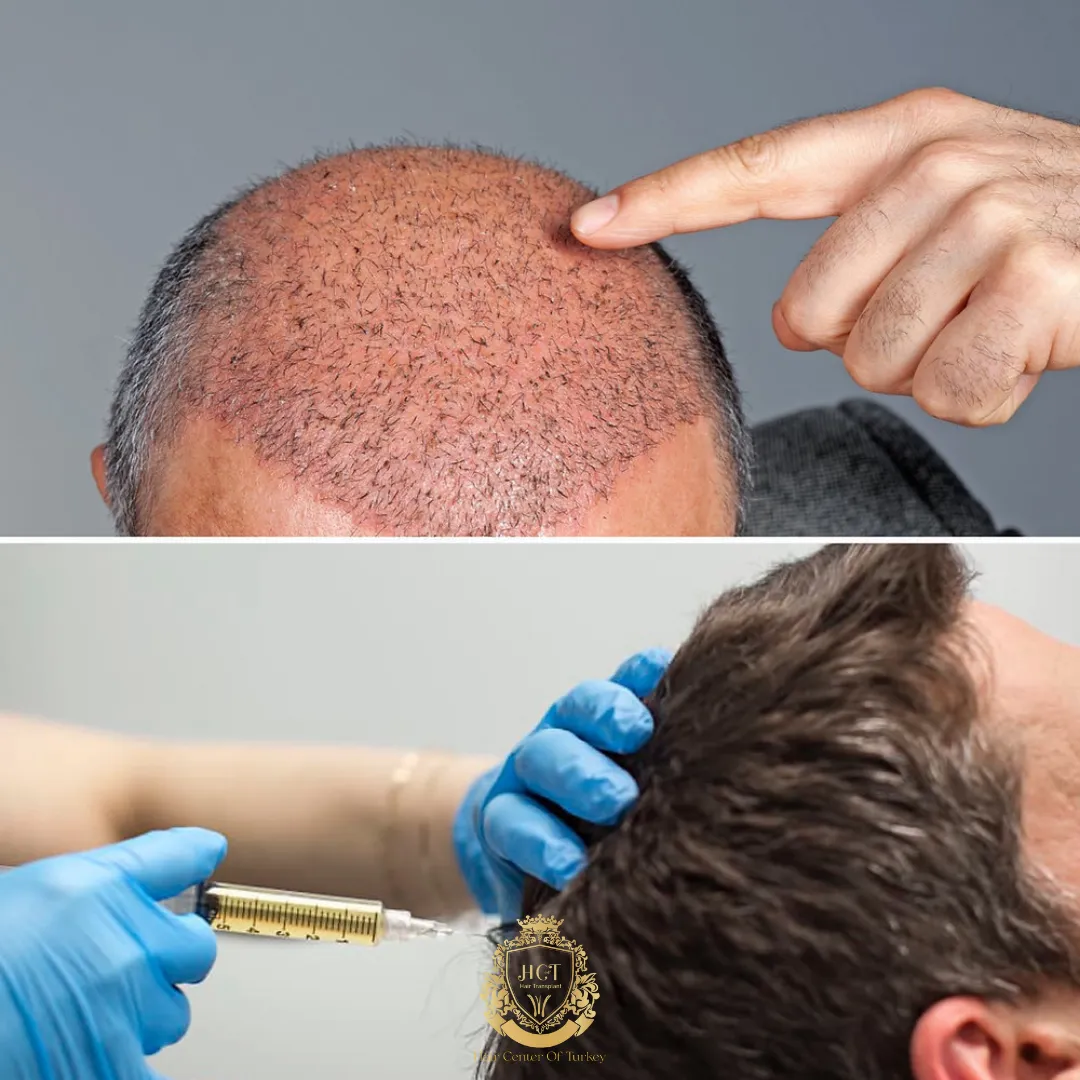
Haarclonering
Haarclonering is een onderzoeksgerichte benadering die erop gericht is nieuwe, transplantabele haarfollikels te creëren door haarvormende cellen in een laboratorium te vermenigvuldigen. In tegenstelling tot FUE of DHI is het ontworpen om de beperkingen van het donorgebied te verminderen of zelfs te elimineren. In 2026 is het nog steeds experimenteel, maar vooruitgang in 3D-celkweek en follikelengineering houdt het in beeld voor toekomstige haarherstelmogelijkheden.
Wat haarclonering betekent bij haarherstel
Bij haarherstel is “haarclonering” een verzamelnaam voor technieken die proberen haarfollikelvormende cellen te vermenigvuldigen en te gebruiken om nieuwe follikels te genereren. Het doel is eenvoudig: meer bruikbare grafts creëren dan de hoofdhuid van nature levert. Het wordt ook wel haarfollikelclonering of haarmultiplicatie genoemd.
De meeste klinieken kunnen momenteel geen echte haarclonering aanbieden. Wat in veel markten beschikbaar is, zijn regeneratieve aanvullingen (bijvoorbeeld PRP of bepaalde producten afgeleid van stamcellen) die bestaande follikels kunnen ondersteunen, maar geen volledig nieuwe creëren.
Inhoudsopgave
Hoe haarclonering zou kunnen werken
1) Kleine biopsie en isolatie van cellen
Een arts neemt een klein stukje weefsel uit een donorgebied waar de follikels genetisch resistent zijn tegen dunner worden. In het laboratorium worden belangrijke celpopulaties geïsoleerd, vaak inclusief cellen gerelateerd aan de dermale papil en ondersteunende follikelcellen. Deze cellen dragen de signalen die haargroei “aansturen”.
2) Celvermeerdering en follikelengineering
De geïsoleerde cellen worden vermeerderd onder gecontroleerde omstandigheden. Onderzoekers gebruiken vaak 3D-kweekmethoden om de cellen zich meer te laten gedragen zoals ze dat in de hoofdhuid doen. In sommige benaderingen worden meerdere celtypen gecombineerd om een follikelachtig structuur te vormen, in plaats van één celtype te injecteren.
3) Implantatie en groeicyclus
Als een stabiele, haarinducerende eenheid kan worden gecreëerd, zou deze in uitgedunde gebieden worden geïmplanteerd. Nieuwe follikels zouden nog steeds de normale groeicycli en uitvalfasen moeten doorlopen. Langdurige overleving, natuurlijke groeirichting en consistente dichtheid zijn belangrijke criteria.
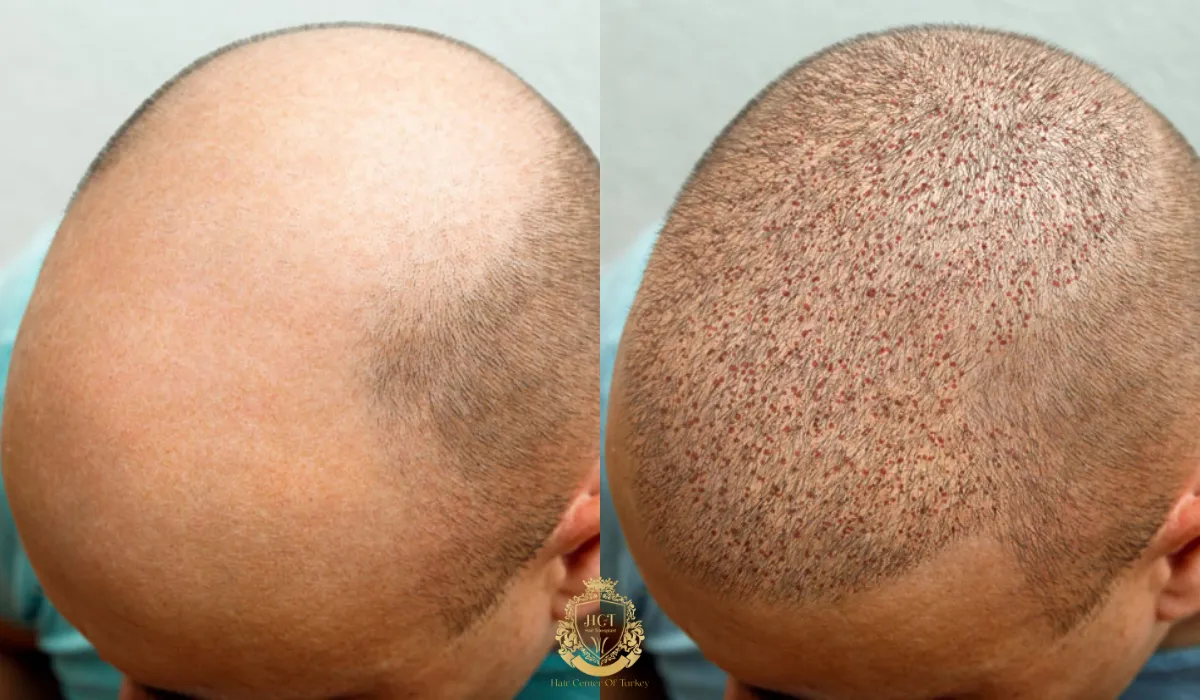
Haarclonering vs. FUE en DHI-haartransplantatie
FUE en DHI herverdelen bestaande follikels. Het aantal grafts dat kan worden verplaatst is beperkt door donordichtheid, hoofdhuidelasticiteit en veilige extractiegrenzen. Haarclonering probeert de beschikbaarheid te vergroten door nieuwe follikels te creëren uit een kleine initiële monstername.
Dat verschil is vooral belangrijk bij gevorderd haarverlies, herstelprocedures en patiënten met beperkte donorreserves. Het verandert ook hoe chirurgen dichtheid en dekking plannen, aangezien de beperkende factor kan verschuiven van donorvoorraad naar de biologie van het ontvangstgebied en de plaatsingsstrategie.
Mogelijke voordelen als de wetenschap zich vertaalt naar patiënten
Als haarclonering klinisch betrouwbaar wordt, zou het de betekenis van “voldoende grafts” kunnen veranderen. In theorie zou het meer opties kunnen bieden voor mensen die momenteel geen goede kandidaten zijn voor chirurgie. Het kan ook de druk verminderen om donorgebieden overmatig te benutten.
De meest besproken potentiële voordelen zijn onder andere:
- Meer graftbeschikbaarheid voor gevorderd haarverlies
- Minder afhankelijkheid van donordichtheid en hoofdhuidkenmerken
- Mogelijkheid om dichtheid te verbeteren zonder agressieve extractie
- Potentieel voor consistentere graftkwaliteit bij gestandaardiseerde protocollen
Uitdagingen en huidige beperkingen
Haarinductieve cellen buiten het lichaam functioneel houden
Een belangrijke uitdaging is dat haarinducerende cellen hun vermogen om follikels te vormen kunnen verliezen in standaard laboratoriumomstandigheden. Veel teams richten zich nu op 3D-sferoïden en micro-omgevingssignalen om dit vermogen te behouden of te herstellen. Zelfs dan is het moeilijk om labresultaten betrouwbaar te vertalen naar menselijke uitkomsten.
Een compleet follikelmicro-omgeving opbouwen
Een haarfollikel bestaat niet uit één celtype. Het is een gecoördineerd mini-orgaan dat afhankelijk is van epithelium-mesenchymale interacties, lokale immuunsignalen, bloedvoorziening en een ondersteunende niche. Het op schaal nabootsen van deze complexiteit is een van de redenen waarom de tijdlijnen onzeker blijven.
Veiligheid, regelgeving en productie
Elke therapie die cellen kweekt of manipuleert moet voldoen aan strikte veiligheidsnormen, waaronder steriliteit, genetische stabiliteit en langdurige monitoring. Benaderingen met pluripotente stamcellen vereisen extra controle vanwege het risico op ongewenste groei. Productie op klinische schaal vereist daarnaast consistente GMP-processen.
Kosten en toegankelijkheid
Vroege versies van celtherapieën zijn meestal duur vanwege laboratoriumwerk, kwaliteitscontrole en regelgeving. Zelfs als haarclonering effectief blijkt, zullen de prijzen aanvankelijk waarschijnlijk hoog zijn voordat bredere toepassing en concurrentie de kosten verlagen.
Huidige vooruitgang in haarclonering in 2026
Onderzoek heeft zich gestaag ontwikkeld richting methoden die de omgeving van de hoofdhuid beter nabootsen. 3D-dermale papilsferoïden, co-kweeksystemen en organoïde-achtige modellen tonen sterkere haarinductiesignalen dan oudere 2D-kweekbenaderingen. Recente overzichtsstudies benadrukken de vooruitgang, maar ook de kloof tussen proof-of-concept en routinematig klinisch gebruik.
Daarnaast zijn er verschillende klinische studies die celgebaseerde of regeneratieve producten voor haarverlies onderzoeken. Deze proeven kunnen inzicht geven in dosering, veiligheid en responsmarkers, maar zijn niet hetzelfde als breed beschikbare “haarclonering” die op aanvraag nieuwe follikels creëert.
Conclusie: haarclonering blijft in 2026 experimenteel. Patiënten moeten op hun hoede zijn voor klinieken die het als een gevestigde behandeling promoten.
Wie mogelijk baat heeft bij haarclonering als het beschikbaar wordt
Als de technologie zich ontwikkelt, kan ze het meest waardevol zijn voor mensen met gevorderde androgene alopecia die niet genoeg donorgebied hebben voor een traditionele transplantatie. Het kan ook helpen bij complexe herstelprocedures waarbij de donorreserves al zijn benut. De uiteindelijke geschiktheid hangt nog steeds af van de gezondheid van de hoofdhuid, de medische voorgeschiedenis en realistische dichtheidsdoelen.
Veelgestelde vragen
Is haarklonen al mogelijk?
Nee, haarklonen is klinisch nog niet beschikbaar.
Hoe lang blijft haarklonen resultaat?
Duur is onbekend wegens ontbrekende goedkeuring.
Wat is de 2026 remedie tegen kaalheid?
Er is geen goedgekeurde remedie in 2026.
Is haarklonen binnen 10 jaar beschikbaar?
Beschikbaarheid binnen 10 jaar is onzeker.
Wordt mannelijke kaalheid genezen tegen 2030?
Waarschijnlijk niet volledig genezen tegen 2030.
Wat gebeurt 20 jaar na haartransplantatie?
Getransplanteerd haar blijft; natuurlijk haar kan dunner worden.
Worden haartransplantaties beter over 10 jaar?
Ja, technieken zullen precisie en resultaten verbeteren.




